NREM 睡眠与 REM 睡眠
这段文字选自《睡眠的科学》,作者:彼得·沃兹尼亚克(2017)
NREM 与 REM 的交替
在一整夜的睡眠过程中,我们会交替进入两种睡眠阶段:
这些 NREM 与 REM 片段的相互作用,对于理解睡眠中的记忆优化、创造力以及解决问题至关重要。
借助 EEG 测量,科学家能够区分 4 个 NREM 睡眠阶段,它们对应着越来越深的睡眠。在较新的文献中,你可能会读到 3 个阶段,这是因为 NREM 的第 3 阶段与第 4 阶段已被合并为单一的慢波睡眠阶段。
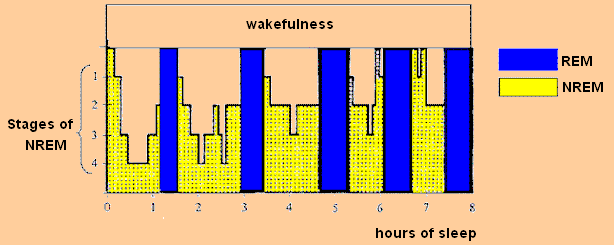
典型夜晚中的 NREM-REM 循环。
当我们闭上眼睛后,通常需要 3–15 分钟进入第 1 阶段 NREM 睡眠(针对健康且调节良好的人)。在这一阶段,我们常会体验到与「下坠感」相关的小抽动。轻微的干扰就会把我们唤醒,我们甚至常常会否认自己睡着了。一旦第 1 阶段 NREM 稳定下来,我们就会进入仍然相对较浅的第 2 阶段 NREM 睡眠。之后我们会进入第 3 阶段(以及第 4 阶段)NREM,也被称为深睡或慢波睡眠(SWS)。
从历史上看,在我们真正意识到慢波睡眠的作用之前,REM 睡眠对记忆与学习的重要性就已被记录下来。因此,与(SWS)相比,关于睡眠的文章与书籍中到处都能见到对 REM 睡眠在学习中作用的过度强调。随着时间推移,REM 剥夺研究受到了大量批评。如今我们知道:连续不中断的 NREM 与 REM 睡眠之间自然、和谐的相互作用,对于记忆、学习与创造力都至关重要(Salzarulo et al. 2000[108])。
残酷的睡眠剥夺研究实际上显示:与剥夺 NREM 相比,剥夺 REM 的睡眠剥夺大鼠反而能活得更久。被剥夺睡眠的大鼠只能存活 2–3 周。而只被剥夺 REM 睡眠的大鼠则能存活大约 5 个月。
午睡的受试者报告说:第 4 阶段 NREM 最让人觉得恢复精力。去甲肾上腺素、血清素与组胺的释放在 REM 期间会受到抑制。做梦时,初级视觉皮层并不活跃,而它的次级区域会活跃。这类似于:人们被要求想象一个视觉场景,与人们真正看到该场景时的情况之间的区别。盲人的梦更偏向听觉与触觉。这似乎印证了 REM 睡眠在体验回放与记忆优化中的作用;他们在 REM 睡眠中也不会呈现典型的眼动模式。这些观察促成了一种观点:与 NREM 睡眠相比,REM 睡眠对创造力更为关键。在 REM 期间,胆碱能调制会抑制信息从海马体流向新皮层。这被认为会帮助在新皮层区域内部建立新的关联。
NREM 与 REM 的演化
与 NREM 睡眠相比,REM 睡眠在系统发育上更「年轻」。鱼类、两栖类或爬行类并不表现出典型的 REM 睡眠。然而有趣的是,REM 睡眠在哺乳动物与鸟类中都存在。这使一些科学家假设:REM 睡眠在进化中曾被「发明」过两次!显然,REM 睡眠对具有鸟类—哺乳动物水平智商的生物的生存至关重要(见:动物睡多少?)。然而,研究了针鼹 REM 睡眠的 Siegel 博士认为,这种动物的睡眠同时具备 REM 与 NREM 睡眠的特征。因此,他提出:REM 与 NREM 可能是从一种在系统发育上更古老、尚未分化的统一睡眠形式演化而来(Siegel et al. 1996[109])。如果 REM 睡眠在功能上与 NREM 如此不同,而且如睡眠中的神经优化相关理论所暗示的那样复杂,那么「再发明」这一因素可能会被进化论者当作反对神经优化的论据。然而,像空中飞行一样,「再发明」与复杂性并存,或许同样能为强调睡眠的关键神经功能提供支持。
NREM 与 REM 的缺口
残酷的睡眠剥夺研究实际上显示:与剥夺 NREM 相比,剥夺 REM 的睡眠剥夺大鼠反而能活得更久。被剥夺睡眠的大鼠只能存活 2–3 周。而只被剥夺 REM 睡眠的大鼠则能存活大约 5 个月。睡眠剥夺之后,最先被偿还的是(SWS)缺口。(SWS)缺口源自 NREM 的睡眠剥夺。REM 的缺口会在之后被偿还。常见情形是:(SWS)缺口在恢复睡眠的第 1 个夜晚就被完全偿还,而 REM 睡眠缺口可能会持续到第 2 个恢复夜晚。
强迫去同步(forced desynchrony)方案是一类睡眠实验方案,在这种方案中,受试者的睡眠会与其自然的昼夜节律周期脱钩。在强迫同步(forced synchrony)条件下,我们可以观察到:表征 NREM 睡眠的慢波活动与稳态睡眠倾向相关,而睡眠片段中 REM 睡眠所占比例则同时依赖稳态压力与昼夜节律周期。
NREM 的控制
NREM 睡眠主要通过稳态机制来控制。在清醒的白天,我们会累积启动睡眠及其更深 NREM 阶段的压力。如果在缺少昼夜节律成分贡献的情况下启动睡眠,它很可能很短,并且只包含 NREM。与稳态困倦相关的信号之一,是腺苷的累积。咖啡因作用于腺苷受体,从而在短时间内减弱稳态睡眠压力。腺苷累积的一个结果,是单胺能清醒中枢受抑、基底前脑受抑,以及 VLPO 去抑制:VLPO 是负责启动睡眠的主要脑区。REM 睡眠也有一个稳态成分;然而在出现缺口时,最先被补偿的是 NREM 睡眠缺口。还有更多证据表明:REM 睡眠会增加 NREM 睡眠压力(Beersma et al. 1990[110])。除腺苷之外,白细胞介素-1、肿瘤坏死因子、干扰素、前列腺素 D2、NO、GHRH 等信号也与稳态睡眠倾向的增加相关(Krueger et al. 2008[111])。
睡眠剥夺会同时增加 NREM 与 REM 睡眠倾向。短睡者的 NREM 2 更少,但关于其睡眠的实际质量与有效性的数据很少。一方面,Thomas Edison 或 Nicola Tesla 以相对睡得少而闻名;另一方面,Einstein 则是著名的长睡者,据说他每晚睡超过 9 小时。有趣的是,这些天才也都属于知名的午睡者。确实,少睡会压缩不那么关键的 NREM 2 睡眠,但没有证据表明:在不伤害 NREM-REM 相互作用质量的前提下,这能成为你的长期习惯。基于目前可获得的睡眠数据,结论是:不要试图通过少睡来压缩 NREM 2。你很可能会损害睡眠中发生的记忆优化过程。
一些科学家认为:在睡眠期间,中脑-脑桥交界处的一个超日节律振荡器(ultradian oscillator)控制着 NREM 与 REM 睡眠的规律交替。然而,「振荡器」这一术语其实会误导人,因为 NREM-REM 的相互作用机制更像一种翻转开关,而且交替的时序相当不规则,这表明存在显著的内部与外部稳态影响,并最终在睡眠周期的终止中达到顶点。
睡眠中的神经调制
睡眠的 AIM 模型(Hobson et al. 2000[79])强调:在缺乏单胺能活动的情况下,主导 REM 的胆碱能调制具有重要意义。
在 NREM 睡眠中,脑干与前脑的胆碱能系统比清醒时更不活跃;5-羟色胺能的中缝核(raphe)与去甲肾上腺素能的蓝斑核(LC)也更不活跃。另一方面,在 REM 睡眠中,这些单胺能结构会被强烈抑制,而胆碱能系统会显著增强。组胺的释放在 REM 中也会下降。有一种假说认为:胆碱能调制会抑制信息从海马体流向新皮层。这被认为在学习的双网络理论模型中扮演重要角色:其中海马体会基于旧信息来建立新的关联(见:睡眠中的神经优化)。
不相信睡眠在记忆与学习中发挥作用的 Siegel 博士认为:REM 睡眠用于恢复,因为 5-羟色胺能、去甲肾上腺素能与组胺能神经元会停止放电,仿佛它们被过度使用,需要补充资源。该解释可能通过「关闭测试」(见:睡眠理论),因为其中许多神经元对维持觉醒至关重要。然而,很难想象进化不会找到一种改造大脑的方法,使神经递质的补充可以在不「关闭」的情况下发生。大脑的一些区域在清醒以及睡眠的所有阶段都会持续放电;相关神经元可以在不停机的情况下补充资源。
生长激素与皮质醇
除了释放不同类型神经递质的神经元放电模式发生变化之外,全身性激素的循环在睡眠中也会改变。其中,生长激素与皮质醇尤为重要,因为它们会影响葡萄糖代谢。生长激素在入睡时上升,并在更深的 NREM 阶段达到峰值。另一方面,皮质醇水平在夜晚后期、以 REM 睡眠为主导的阶段上升。与主要由昼夜节律驱动的皮质醇释放不同,生长激素的上升与入睡相关(Van Cauter et al. 1997[112])。睡眠剥夺或在错误的相位睡觉,都会以不同原因严重扰乱葡萄糖代谢。这就是为什么健康睡眠对预防肥胖至关重要。
REM 稳态
总体而言的睡眠与之类似,REM 也通过稳态与昼夜节律过程来控制。昼夜节律 REM 周期的顶峰相位(Acrophase)出现在主观夜晚的后段。Benington 与 Heller 提出:导致 REM 睡眠倾向增加的,是 NREM 睡眠的存在,而不是 REM 睡眠的缺失。慢波睡眠会建立稳态的 REM 倾向,而最好的 REM 来自慢波的「耗竭」与睡眠最后几小时出现的昼夜节律 REM 峰值的结合。学习与 REM 睡眠需求之间也存在强烈的稳态联系:你学得越多,趋向 REM 的驱动力就越强。高强度学习后,REM 睡眠的分钟数与 REM 密度都会增加(De Koninck et al. 1989[113])。目前尚不清楚学习是直接影响 REM 需求,还是通过影响 NREM 需求而间接影响。不过,有一点非常明确:重度学习者就应该是重度睡眠者!
刺激基底前脑会释放乙酰胆碱,它会诱发清醒状态,也有利于 REM 睡眠。这意味着:参与入睡启动的基底前脑也参与 NREM/REM 的转换。同样,VLPO 的一部分细胞群也会参与生成 REM 睡眠。
像咖啡因这样的腺苷拮抗剂也会产生重要影响。将腺苷激动剂灌注到基底前脑,会增加 VLPO 中的 c-Fos,并增加基底前脑释放乙酰胆碱。众所周知,乙酰胆碱会诱发清醒状态与 REM 睡眠。由于灌注激动剂,NREM 与 REM 的总量都会增加(Satoh et al. 1999[105],Scammell et al. 2001[87])。
在其他稳态激素影响方面,睡眠中 VIP 与催乳素水平升高会促进 REM。物质滥用、推迟入睡以及使用闹钟,都可能导致 REM 睡眠缺口(见:REM 反弹假说)。
有一种睡眠理论认为,REM 睡眠帮助大脑从 NREM 睡眠中恢复,从而加快清醒时的反应。这一理论无法通过关闭测试,因为同样的恢复完全可以在清醒状态下发生,除非做梦时神经网络的「重活」在某种未知意义上是一种更快的恢复方式。然而,为什么在「完全恢复」到清醒的条件下,大脑还会出现 REM 反弹?认为组胺、血清素与去甲肾上腺素神经元需要恢复时间的说法更可信;但这仍无法解释:为什么我们需要不同的神经元群体、不同的神经递质,以及不同的修复与恢复策略。
向 REM 的过渡
在主观夜晚睡眠期间,经历大约 1 小时左右的健康 NREM 睡眠后,脑桥被盖细胞的活动会逐渐增强,而该区域负责触发 REM 睡眠。负责触发 REM 睡眠的结构可能包括脚桥被盖核(PPN)与亚外侧背核(SLD)。GABA 能的 SLD 与胆碱能的 PPN 会把信号向多个方向发送。其结果之一是肌张力消失;另一个结果是激活丘脑、海马体与大脑皮层,并出现典型的 REM EEG。结果是,大脑表现得仿佛在内部「醒来」了!在一次持续的 NREM 片段期间,将乙酰胆碱注入脑桥可能触发 REM 睡眠,这说明该神经递质在睡眠周期调节中的重要性。在 REM 睡眠期间,皮层的行为与清醒状态相似。此阶段的梦似乎由从脑干发送到皮层的随机冲动生成。皮层会为这些混乱的输入生成尽可能好、尽可能连贯的图像。在梦中,我们会经历连续的事件、真实的人、逼真的景观等。然而,这些元素会以最不可能的组合被拼接在一起,仿佛大脑在测试「如果……会怎样」的情景。尽管如此,我们却无法对梦采取行动(除非是患有睡眠中暴力行为的人)。负责控制 REM 的脑桥结构会确保大脑输出与控制肌肉运动的运动核团隔离。我们在睡眠中经常想要行动(例如逃离一只凶猛的狗),但却会像陷在糖浆里一样一动不动。此时,只有眼睛会快速运动,同时中耳的肌肉也会抽动。
赋予 REM 这一名称的眼球运动,由在脑桥核中产生并投射到上丘(superior colliculi)的冲动所控制。该冲动与脑桥-外侧膝状体-枕叶波(PGO 波)的生成相关;PGO 波也可用于检测 REM 睡眠。
做梦时,初级视觉皮层并不活跃,而它的次级区域会活跃。这类似于:人们被要求想象一个视觉场景,与人们真正看到该场景时的情况之间的区别。盲人的梦更偏向听觉与触觉。这似乎印证了 REM 睡眠在体验回放与记忆优化中的作用;他们在 REM 睡眠中也不会呈现典型的眼动模式。这些观察引出了一种观点:与 NREM 睡眠相比,REM 睡眠对创造力更为关键。
REM 翻转开关
NREM 与 REM 睡眠的相互作用,很可能由一个 REM 翻转开关控制。一些科学家认为:在睡眠期间,中脑-脑桥交界处的一个超日节律振荡器控制着 NREM 与 REM 睡眠的规律交替。然而,考虑到交替发生的时序,翻转开关模型是更好的类比。
如同睡眠-觉醒翻转开关一样,REM 翻转开关会在相对稳定的 NREM 与 REM 状态之间不断切换。不过,与睡眠-觉醒翻转开关相比,REM 翻转开关受到更多稳态输入的影响,导致 NREM/REM 状态的更迭有些混乱;而在主观夜晚结束前夕,这种更迭会逐渐被 REM 的昼夜节律峰值所主导。
在许多年里,胆碱能与单胺能状态之间的振荡曾被认为是控制 REM 睡眠的最终答案。然而,一些不一致之处与新研究促使人们提出了一个类似的新模型,其中涉及 GABA 能结构(见下一节)。
REM 翻转开关模型
1962 年,Jouvet 证明:刺激猫的尾侧中脑区域或脑桥被盖会产生一种类似 REM 睡眠的状态。这引出了一个假说:位于中脑-脑桥的胆碱能结构负责在 REM 睡眠中激活丘脑与大脑皮层。该假说也可以由如下事实支持:将胆碱能激动剂注射进脑桥网状结构会增强 REM 睡眠。
原始的「互惠相互作用模型」认为:脑桥的单胺能与胆碱能神经元形成了经典的 REM-on/REM-off 翻转开关。该模型在长达四分之一个世纪里被当作事实接受。新研究则识别出可能位于开关两侧(on 与 off)并参与 REM 翻转开关的 GABA 能神经元群体。
旧的 REM 翻转开关包含胆碱能的 脚桥核(PPT) 与 被盖(LDT)(它们在 REM 期间以及清醒时都特别活跃),以及 BRF(脑干网状结构)。REM-off 组成部分包括 中缝背核DR(血清素)以及 蓝斑核LC(NA)(Saper et al. 2001[114])。
较新的研究质疑了该模型中的一些不一致之处。例如,对脑干胆碱能或单胺能核团进行选择性损毁,对 REM 睡眠只有有限影响。REM 期间 REM-on 结构中的 c-Fos 表达偏低也令人困扰。于是有人提出,关键的 REM-on 区域其实是 GABA 能的 SLD(亚外侧背核)(Lu et al. 2007[115])。由于 SLD 并不直接抑制 DR-LC,人们也因此质疑它们是否直接参与翻转开关。SLD 的 GABA 能神经元会投射到 vlPAG(腹外侧导水管周围灰质)与 LPT(外侧脑桥被盖),从而使它们成为 REM-off 的嫌疑对象。对 SLD 的损毁会导致 REM 睡眠丧失。
REM 翻转开关的精确性质仍有待确定。旧模型与新模型的组成部分之间也存在一定相互作用。例如,PPT/LDT 确实会兴奋 SLD 神经元,而 DR/LC 可能抑制 SLD 或激活 REM-off 组成部分。然而,这种相互作用并不是直接的互惠关系。因此,旧模型的组成部分被排除在新模型核心之外。
睡眠的终止
如果没有睡眠驱动力中的昼夜节律成分,睡眠控制系统就会像一个无穷无尽的跷跷板一样运作。到睡眠末期,由视交叉上核(SCN)所决定的昼夜节律困倦会导致睡眠倾向下降,睡眠会在某一次 REM 睡眠片段之后终止。SCN 提供了最强授时因子——光——与昼夜节律周期之间的联结。SCN 在体内生成节律,但也能被光重置。来自视网膜的光脉冲会传至下丘脑与 SCN,从而产生一个停止并重置(stop&reset)的信号。睡眠结束时,褪黑素释放也随之结束;相反,另一种神经激素开始累积:血清素。有一种假说认为,我们把高水平血清素体验为清晨阳光带来的幸福感。高水平血清素与警觉激素皮质醇结合,会让我们以良好的警觉状态开启新的一天。除非你遭受睡眠相位提前,否则请始终确保清晨的阳光能照进你的卧室,把你唤醒。